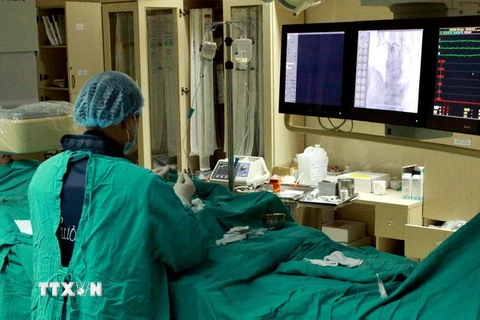
(Ảnh minh họa: TTXVN)
(Ảnh minh họa: TTXVN) Tiến hành thử nghiệm lâm sàng các loại thuốc như thế nào? Có cần đưa ra thời hạn cho một nhãn hiệu sản phẩm dược? Có sự khác biệt nào trong chính sách ưu tiên giữa doanh nghiệp trong và ngoài nước?… Đó là hàng loạt các vấn đề đã được các chuyên gia Việt Nam và quốc tế đặt ra tại Hội thảo Chia sẻ kinh nghiệm xây dựng Luật Dược với mục tiêu vì người bệnh.
Hội thảo do Bộ Y tế phối hợp với Pharna Group tổ chức sáng nay, ngày 9/10, tại Hà Nội.
Chậm nhất ASEAN
Phát biểu tại Hội thảo, ông Anthony Morton Samll, Giám đốc Hợp danh cao cấp của Tập đoàn tư vấn IMS, văn phòng Châu Á- Thái Bình Dương tại Singopore, chuyên gia tư vấn cho các công ty đa quốc gia và doanh nghiệp hoạt động trong lĩnh vực dược, thiết bị y tế, cho biết, IMS đã tiến hành nghiên cứu độc lập về khả năng sẵn có và chấp nhận thuốc phát minh mới tại Việt Nam.
Nghiên cứu này dựa trên dữ liệu doanh số của dược phẩm trên toàn cầu để so sánh trên phạm vi quốc tế giữa Việt Nam và các nước khác.
Kết quả nghiên cứu cho thấy Việt Nam là nước có thời gian lâu nhất cho việc đưa một hoạt chất mới trên thế giới vào thị trường trong nước.
Cụ thể, thời gian trung bình để đưa một hoạt chất mới ra thị trường ở Việt Nam tính từ lúc hoạt chất này lần đầu tiên đưa ra thị trường thế giới là 5,4 năm, lâu nhất trong các nước ASEAN. Khoảng thời gian này ở Malaysia chỉ 3,2 năm, ở Philippine là 3,3 năm, Indonesia là 3,5 năm, Thái Lan là 3,7 năm.
Vì lý do này, số hoạt chất mới có mặt ở Việt Nam khá khiêm tốn.
Trong số 143 hoạt chất mới được giới thiệu từ năm 2007 đến năm 2011 trên thế giới, hiện chỉ có 21 hoạt chất có mặt tại Việt Nam.
Tuy nhiên, ông Cường cho biết, Việt Nam đã nhận ra đây điểm bất hợp lý trong điều kiện hiện tại, và vì thế, trong dự thảo Luật Dược mới đã bỏ quy định này. Theo đó, thời gian tới, các thuốc mới, nhất là các nước đã được đưa vào các nước tham chiếu như Nhật Bản, các quốc gia EU… sẽ được đưa vào Việt Nam sớm hơn.
Cũng tại hội thảo, nhiều đại biểu đã nêu ra một số kết quả đã đạt được của Luật Dược năm 2005. Sau 10 năm, từ chỗ chỉ có có khoảng 50 cơ sở đạt tiêu chuẩn GMP ASEAN, đến nay, số lượng cơ sở sản xuất thuốc đạt WHO-GMP là 142 cơ sở (với 154 nhà máy), trong đó có một số cơ sở đạt EU-GMP, GMP-PIC/s.
Năm 2005, thuốc sản xuất trong nước có hơn 300 hoạt chất nhưng hiện nay con số này đã là 500 hoạt chất. Sản xuất thuốc trong nước đạt tỷ lệ tăng trưởng bình quân trung bình trên 15% trong khi tăng trưởng GDP của cả nước đạt khoảng 6%.
Tuy nhiên, sau 10 năm thực thi, Luật Dược cần được sửa đổi cho phù hợp với tình hình thực tiễn, giúp người dân tiếp cận thuốc mới nhanh hơn và hội nhập quốc tế.
 Nghiên cứu, sản xuất thuốc mới trong nước. (Ảnh: TTXVN)
Nghiên cứu, sản xuất thuốc mới trong nước. (Ảnh: TTXVN) Dự thảo Luật đã có sự tương đồng với quốc tế
Tại Hội thảo, các chuyên gia cũng đã nêu các kinh nghiệm quốc tế trong các vấn đề liên quan đến dược cách quản lý của châu Âu về quản lý nhà phân phối dược phẩm, về yêu cầu thử nghiệm lâm sàng trước khi sử dụng ở một địa phương…
Vấn đề được nhiều đại biểu quan tâm là châu Âu có quy định về thời hạn đăng ký lưu hành của một loại thuốc không? Có được đăng ký lại không? Nhà phân phối thuốc được quản lý thế nào? Có phải thử nghiệm lâm sàng các loại thuốc đã được sử dụng ở các nước khác trước khi cho lưu hành trong nước hay không?...
Theo ông Pieter Neels, nguyên thành viên Ủy ban các sản phẩm y tế nhân sinh, nguyên Phó chủ tịch Ban Công tác vắcxin, Cơ quan quản lý dược phẩm châu Âu, tại EU, cho rằng các kết quả thử nghiệm từ các nước khác chỉ được chấp nhận với điều kiện các nước đó có điều kiện thực hiện đánh giá chặt chẽ.
“Tại EU, ngay cả sau khi cấp phép thuốc vẫn được nghiên cứu về hiệu quả và độ an toàn,” ông Pieter Neels nói.
Cũng theo ông Pieter Neels, các sản phẩm thuốc ở châu Âu chỉ được cấp phép lưu hành 5 năm. Sau 5 năm, cơ sở sản xuất thuốc phải làm báo cáo với những bằng chứng cụ thể về tình hình sử dụng, hiệu quả của thuốc để được cấp phép lại.
Bổ sung thêm về vấn đề này, ông Fernand Sauer, nguyên Giám đốc cơ quan quản lý dược phẩm châu Âu, cho biết, các nhà sản xuất hay nhập khẩu, buôn bán hóa dược tại châu Âu cũng phải được đăng ký với các điều kiện chặt chẽ.
“Các điểm bán thuốc đều phải đạt yêu cầu về cơ sở vật chất như điều kiện bảo quản thuốc, trình độ của người bán thuốc và được thanh kiểm tra định kỳ. EU cũng áp dụng một logo chung cho các nhà thuốc, nhà bán lẻ trực tuyến hoạt động hợp pháp ở các nước thành viên để tránh tình trạng bán thuốc bất hợp pháp,” ông Fernand Sauer nói.
Theo ông Trương Quốc Cường, Cục trưởng Cục Quản lý dược, Bộ Y tế, các quy định của Việt Nam trong dự thảo Luật Dược mới cũng có nhiều điểm tương đồng với quốc tế. Chẳng hạn như quy định về thời hạn đăng ký lưu hành cho sản phẩm thuốc là 5 năm, sau đó doanh nghiệp phải có báo cáo để có thể đăng ký lại.
Việt Nam cũng có quy định chặt chẽ về các yêu cầu cơ sở vật chất, trình độ với các dược sỹ tại các điểm bán thuốc…
“Những kinh nghiệm của quốc tế được chia sẻ tại Hội thảo hôm nay sẽ giúp Việt Nam hoàn thiện hơn dự thảo Luật Dược để trình Quốc hội trong thời gian tới,” ông Cường nói./.