 Ảnh minh họa. (Nguồn: trialsitenews.com)
Ảnh minh họa. (Nguồn: trialsitenews.com)
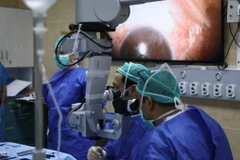
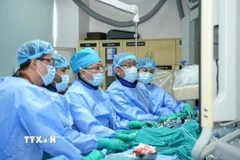
Ban cố vấn của Cơ quan Quản lý thực phẩm và dược phẩm Mỹ (FDA) đã khuyến nghị tập đoàn sinh học Innovent (Trung Quốc) và hãng dược phẩm Eli Lilly (Mỹ) tiến hành thêm thử nghiệm đối với thuốc điều trị ung thư phổi Sintilimab mà hai hãng trên cùng hợp tác sản xuất.
Trong thông báo ngày 10/2, Ban cố vấn FDA nêu rõ cơ quan này cần Innovent/Eli Lilly cung cấp thêm dữ liệu thử nghiệm, vì loại thuốc này mới chỉ được thử nghiệm ở Trung Quốc.
[Cải thiện chất lượng điều trị cho bệnh nhân mắc ung thư phổi]
Hãng dược phẩm Eli Lilly đã bày tỏ "thất vọng" về kết quả cuộc họp của Ban cố vấn FDA, đồng thời khẳng định sẽ tiếp tục hợp tác cho đến khi cơ quan này hoàn thành việc đánh giá thuốc Sintilimab.
Trong khi đó, Innonvent vẫn khẳng định tin tưởng vào hiệu quả của Sintilimab.
Sau khuyến nghị trên của Ban cố vấn FDA, cổ phiếu của Innovent đã giảm tới hơn 10% trong phiên giao dịch ngày 11/2.
Một số hãng dược phẩm tìm cách đưa sản phẩm thâm nhập vào thị trường Mỹ đã quan ngại khi chỉ tiến hành thử nghiệm lâm sàng tại một nước.
Trong thử nghiệm tại Trung Quốc, Sintilimab được dùng để điều trị bệnh nhân ung thư phổi tiến triển hoặc tái phát.
Thuốc này đạt được mục tiêu chính là thời gian sống bệnh không tiến triển (PFS) hay bệnh tình của bệnh nhân không chuyển biến nặng.
Ngoài vấn đề thiếu sự đa dạng giữa các nhóm bệnh nhân tham gia thử nghiệm, các chuyên gia Mỹ còn quan ngại việc sử dụng PFS làm mục tiêu chính của nghiên cứu thay vì tỷ lệ sống sót tổng thể (OS) - một tiêu chuẩn "vàng" trong việc đánh giá hiệu quả của các loại thuốc chữa trị ung thư./.