Người đứng đầu Cơ quan Thực phẩm và Dược phẩm Mỹ (FDA) Stephen Hahn đã để ngỏ khả năng một vắcxin tiềm năng trong tương lai phòng bệnh viêm đường hô hấp cấp COVID-19 có thể được phê chuẩn khẩn cấp trước khi kết thúc các công đoạn thử nghiệm theo quy định từ trước tới nay nhằm đảm bảo độ an toàn và hiệu quả.
Trả lời phỏng vấn báo The Financial Times, số ra ngày 30/8, ông Hahn cho biết việc đề nghị phê chuẩn khẩn cấp vắcxin sẽ do một công ty phát triển vắcxin đưa ra.
"Nếu họ đề nghị trước khi kết thúc giai đoạn ba, chúng tôi có thể tìm cách thích hợp để ra quyết định," ông Hahn cho biết.
[Mỹ mua toàn bộ 150 triệu xét nghiệm nhanh COVID-19 mới của Abbott Labs]
Tuy nhiên, ông Hahn nhấn mạnh ông không hành động dưới sức ép của Tổng thống Donald Trump, người đã hối thúc đẩy nhanh việc tìm ra vắcxin trước ngày bầu cử tổng thống 3/11 tới.
Ông Hahn khẳng định: "Đây sẽ là một quyết định khoa học, y tế và dựa trên các dữ liệu, không phải là một quyết định mang tính chính trị."
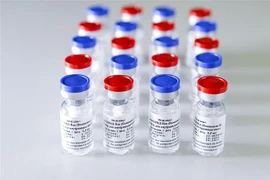
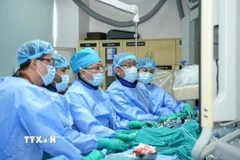
Hiện 3 hãng dược phẩm phương Tây đang thử nghiệm vắcxin giai đoạn 3, cũng là giai đoạn cuối, trên diện rộng để kiểm tra độ an toàn và hiệu quả của vắcxin, với sự tham gia của hàng nghìn tình nguyện viên.
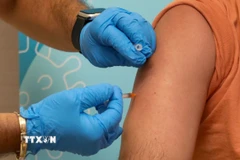
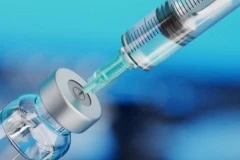
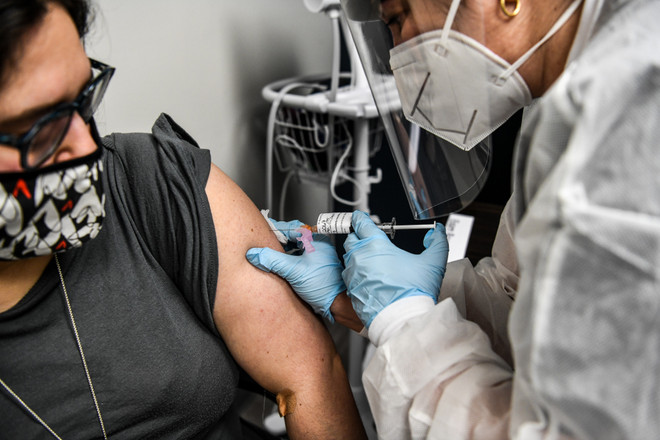 Tiêm vắcxin ngừa COVID-19 cho một tình nguyện viên tại Hollywood, bang Florida, Mỹ, ngày 13/8/2020. (Ảnh: AFP/TTXVN)
Tiêm vắcxin ngừa COVID-19 cho một tình nguyện viên tại Hollywood, bang Florida, Mỹ, ngày 13/8/2020. (Ảnh: AFP/TTXVN)
Đó là vắcxin của công ty Anh-Thụy Điển AstraZeneca phối hợp với Đại học Oxford của Anh bào chế; vắcxin của hãng dược Moderna phối hợp với Viện Y tế quốc gia Mỹ bào chế; và vắcxin của liên minh giữa Pfizer và BioNTech.
Về lý thuyết lâm sàng, khó có thể dự báo khi nào có kết quả chắc chắn. Theo quy trình bình thường, phải mất vài tháng để xem liệu có sự khác biệt đáng kể về số liệu thống kê tỷ lệ nhiễm giữa hai nhóm, gồm một nhóm được tiêm vắcxin thử nghiệm và nhóm khác được tiêm giả dược.
Trong bối cảnh thế giới đang rất cần có một vắcxin hiệu quả phòng virus chết người này, Trung Quốc và Nga đã phê chuẩn vắcxin của mình mà không chờ đến khi kết thúc các thử nghiệm lâm sàng.
Về việc này, ông Hahn cho biết việc FDA có thể phê chuẩn khẩn cấp cho vắcxin nào đó "không đồng nghĩa với việc phê chuẩn đầy đủ"./.