Bộ Y tế Nhật Bản vừa ủng hộ việc cấp phép có điều kiện cho hai loại thuốc tiên phong điều trị bệnh Parkinson và suy tim nghiêm trọng dựa trên công nghệ tế bào gốc.
Theo Nature, dù mang lại niềm hy vọng lớn lao cho nền y học tái tạo, giới khoa học quốc tế đang bày tỏ sự lo ngại sâu sắc vì dữ liệu thử nghiệm lâm sàng hiện tại của hai liệu pháp này còn quá ít ỏi.
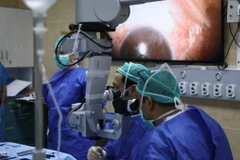
Hai liệu pháp mang tên Amchepry (chữa bệnh Parkinson) và ReHeart (trị suy tim nghiêm trọng) đều ứng dụng công nghệ tế bào gốc đa năng cảm ứng (iPS) - một đột phá khoa học từng đoạt giải Nobel.
Về cơ bản, kỹ thuật này lấy tế bào trưởng thành từ máu của tình nguyện viên, "tái lập trình" chúng thành tế bào iPS, sau đó nuôi cấy thành các tế bào chuyên biệt để cấy ghép lại vào cơ thể người bệnh.
Với liệu pháp Amchepry, các tế bào iPS được phát triển thành tế bào sản sinh dopamine và cấy vào não người bệnh Parkinson. Kết quả thử nghiệm giai đoạn đầu cho thấy thuốc không gây tác dụng phụ nghiêm trọng và giúp giảm triệu chứng run ở ít nhất 4 bệnh nhân.
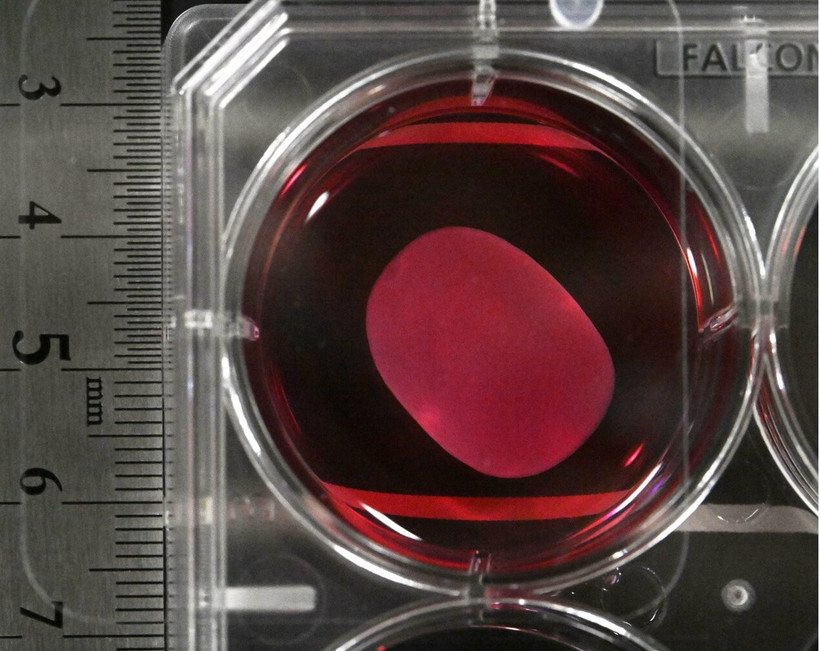
Trong khi đó, với ReHeart, tế bào được biệt hóa thành các miếng vá cơ tim chứa tới 100 triệu tế bào để ghép vào tim bệnh nhân.
Thử nghiệm ban đầu đánh giá ReHeart an toàn và giúp một số người bệnh vận động thể chất tốt hơn.
Tuy nhiên, nút thắt gây tranh cãi nằm ở quy mô thử nghiệm: Amchepry mới chỉ được thử nghiệm trên 7 người, còn ReHeart là 8 người. Cả hai đều không có nhóm đối chứng, khiến việc đưa ra kết luận chắc chắn về hiệu quả thực sự trở nên khó khăn.
Đánh giá về động thái của Nhật Bản, Paul Knoepfler, nhà nghiên cứu tế bào gốc tại Đại học California, Davis (Mỹ), nhận định: "Đây là một thử nghiệm quy định đầy rủi ro."
Ông chia sẻ thêm: "Những dữ liệu mà tôi thấy về các sản phẩm này trông có vẻ đáng khích lệ, nhưng có vẻ như còn quá sớm để nói về việc thương mại hóa những sản phẩm như vậy."
Theo luật pháp Nhật Bản, các loại thuốc y học tái tạo sau khi trải qua thử nghiệm lâm sàng thăm dò có thể được "cấp phép có điều kiện và giới hạn thời gian."
Nếu được chính thức thông qua vào tháng 3 tới, các công ty phát triển có thể bán hai loại thuốc này trong 7 năm cho một lượng bệnh nhân nhất định. Trong thời gian đó, họ sẽ tiếp tục theo dõi phản ứng để đánh giá độ an toàn và hiệu quả.
Đại diện nhà phát triển Amchepry lên tiếng bảo vệ lộ trình này: "Ưu tiên của chúng tôi là tích lũy cẩn thận các bằng chứng lâm sàng chứ không phải mở rộng thị trường."
Dù vậy, bác sỹ phẫu thuật chỉnh hình Hiroshi Kawaguchi tại Bệnh viện Nadogaya (Nhật Bản) cho rằng cơ chế cấp phép này đẩy gánh nặng tài chính và đạo đức sang người bệnh, người nộp thuế và các công ty bảo hiểm.
Hơn nữa, phương pháp này đòi hỏi phẫu thuật xâm lấn, người bệnh phải dùng thuốc ức chế miễn dịch để chống đào thải, và tiềm ẩn nguy cơ các tế bào được tái lập trình biến thành khối u.
Ông cho hay: "Tôi ủng hộ khoa học về tế bào iPS, nhưng tôi đặt câu hỏi về việc thương mại hóa sớm với bằng chứng không đầy đủ."
Hiện có hơn 100 thử nghiệm liệu pháp tế bào gốc đang diễn ra trên toàn cầu, nhưng phần lớn mới ở giai đoạn sơ khai.
Jeanne Loring, nhà nghiên cứu tế bào gốc tại Viện Nghiên cứu Scripps (Mỹ), cảnh báo rằng việc hạ thấp tiêu chuẩn quy định sẽ "mở ra cánh cửa cho công việc cẩu thả và thúc đẩy mọi người làm mức tối thiểu cần thiết để cho thấy rằng liệu pháp của họ là an toàn."
Bà lo ngại rằng nếu bệnh nhân gặp phải các tác dụng phụ nghiêm trọng, điều đó sẽ giáng một đòn mạnh vào toàn bộ lĩnh vực y tế đầy triển vọng này.
Thể hiện sự không đồng tình với cách làm của các công ty, bà Loring thẳng thắn đặt câu hỏi: "Liệu tôi có đồng ý nếu ai đó xuất hiện và nói rằng, tôi đã thử nghiệm tế bào của mình trên 5 bệnh nhân, và tôi muốn được phê duyệt và tôi muốn bạn trả tiền cho việc đó không? Tôi không thích ý tưởng đó"./.

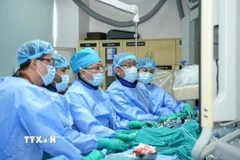
Điều trị bệnh suy tim nặng bằng phương pháp cấy ghép cơ tim từ tế bào iPS
Theo thông báo của Công ty Heartseed, thử nghiệm lâm sàng trên 10 bệnh nhân suy tim nặng cho thấy phương pháp cấy ghép cơ tim từ tế bào iPS giúp cải thiện chức năng tim và các triệu chứng lâm sàng.