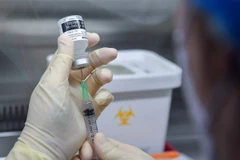
Ảnh minh họa. (Nguồn: The Indian Express)
Ảnh minh họa. (Nguồn: The Indian Express)
Ngày 2/8, Bộ Y tế Ấn Độ đã tiến hành các cuộc kiểm tra trên diện rộng trong toàn ngành dược và phát hiện nhiều sai sót của các nhà sản xuất dược phẩm, bao gồm cả việc không tiến hành kiểm tra nguyên liệu thô.
Thông báo của bộ trên cho biết các cuộc kiểm tra - được tiến hành tại 162 nhà máy và 14 phòng thí nghiệm công, đã phát hiện các vấn đề bao gồm "tài liệu nghèo nàn, thiếu quy trình đánh giá và xác nhận phân tích, không điều tra lỗi chất lượng và không đánh giá chất lượng sản phẩm nội bộ."
Ngoài ra, còn có các vấn đề như không thử nghiệm nguyên liệu thô, thiếu các biện pháp để tránh lây nhiễm chéo, thiếu nhân viên có trình độ chuyên môn và thiết kế sai các khu vực sản xuất và thử nghiệm.
Ấn Độ đã tăng cường giám sát các nhà sản xuất thuốc trong những tháng gần đây, sau khi một số loại siro ho sản xuất tại nước này có liên quan đến cái chết của ít nhất 95 trẻ em ở châu Phi.
Ngành công nghiệp dược phẩm trị giá 41 tỷ USD của Ấn Độ là một trong những ngành lớn nhất toàn cầu, được biết đến với việc cung cấp các sản phẩm thay thế rẻ hơn cho các sản phẩm phương Tây. Nhưng vụ nhiều trẻ em tử vong liên quan đến siro ho gần đây đã làm tổn hại đến hình ảnh này.
[Ấn Độ: Thêm một công ty phải ngừng sản xuất do vụ siro ho nhiễm độc]
Chính phủ Ấn Độ đã yêu cầu 4 công ty dược phẩm ngừng sản xuất thuốc, sau khi Tổ chức Y tế thế giới (WHO) phát hiện chất gây ô nhiễm trong sản phẩm siro ho của họ. Các công ty này phủ nhận cáo buộc.
Ấn Độ đã siết chặt việc kiểm tra xuất khẩu siro ho từ tháng 6, theo đó các công ty dược phải có giấy chứng nhận phân tích từ phòng thí nghiệm của chính phủ trước khi xuất khẩu.
Bộ Y tế Ấn Độ cũng đã nâng cấp các quy định về sản xuất thuốc và mỹ phẩm. Các nhà sản xuất dược phẩm lớn có 6 tháng và các nhà sản xuất nhỏ 12 tháng để đảm bảo tuân thủ quy định nâng cấp mới./.