Cơ quan quản lý dược phẩm châu Âu. (Nguồn: EMA)
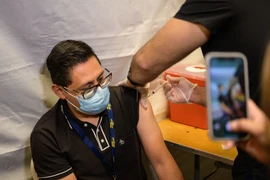
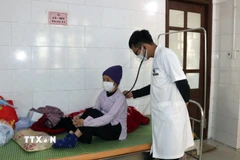
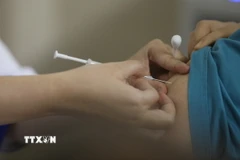
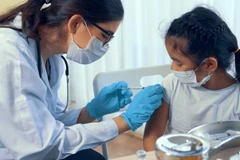
Cơ quan quản lý dược phẩm châu Âu. (Nguồn: EMA)
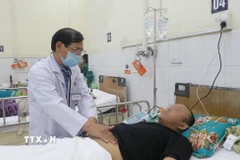
Cơ quan quản lý dược phẩm châu Âu (EMA) ngày 18/11 cho biết đang đánh giá đơn xin cấp phép sử dụng thuốc kháng thể đơn dòng Sotrovimab trong điều trị bệnh COVID-19. Quyết định có thể được đưa ra trong khoảng 2 tháng nữa.
Sotrovimab, có tên thương mại là Xevudy, là thuốc điều trị COVID-19 dạng tiêm do hãng dược phẩm GlaxoSmithKline (GSK) và công ty Vir Biotechnology đồng phát triển.
Nếu được EMA phê chuẩn, đây sẽ là loại thuốc điều trị COVID-19 được cấp phép sử dụng tại châu Âu.
Thuốc Sotrovimab đã được cấp phép sử dụng khẩn cấp tại Mỹ nhằm ngăn chặn các ca bệnh nhẹ hoặc trung bình trở nặng hơn. Hiện tổng số liều thuốc Sotrovimab được đặt mua trên toàn cầu đã lên hơn 750.000.
Mới đây nhất, Mỹ ký hợp đồng trị giá gần 1 tỷ USD để mua Sotrovimab. Trước đó, khoảng 10.000 liều thuốc Sotrovimab được bán cho Canada và 220.000 liều cho EU.
[Kỳ vọng thuốc điều trị COVID-19 làm thay đổi cuộc chiến chống đại dịch]
Trong diễn biến khác, hãng dược phẩm Pfizer cho biết đã ký thỏa thuận với Chính phủ Mỹ để cung cấp 10 triệu lộ trình điều trị COVID-19 bằng loại thuốc kháng virus dạng uống của mình, trị giá 5,29 tỷ USD.
Hợp đồng này có quy mô lớn gấp đôi hợp đồng mà Chính phủ Mỹ đã ký với công ty Merck & Co Inc dù giá thuốc của Pfizer thấp hơn, chỉ khoảng 530 USD/liệu trình so với 700 USD của Merck.
Thuốc mang tên thương mại là Paxlovid, hiện đang ở cấp độ nghiên cứu.
Pfizer đã nộp hồ sơ xin cấp phép sử dụng khẩn cấp Paxlovid trong tuần này sau khi các dữ liệu cho thấy 89% hiệu quả trong việc tránh phải nhập viện hoặc tử vong ở những người có nguy cơ cao.
Pfizer cho biết sẽ bắt đầu giao thuốc ngay trong năm nay nếu được Cơ quan quản lý thực phẩm và dược phẩm Mỹ (FDA) phê chuẩn.
Về phần mình, Bộ trưởng Y tế và Dịch vụ con người, ông Xavier Becerra cho biết: "Thỏa thuận này sẽ giúp đảm bảo hàng triệu liều thuốc sẵn sàng cung cấp cho người dân Mỹ nếu được cấp phép."
Ông nhấn mạnh rằng dù việc tiêm vaccine ngừa COVID-19 là một ưu tiên, nhưng có các viên thuốc có thể giúp mọi người không phải nhập viện cũng "có thể là một cứu tinh".
Pfizer dự định sản xuất 180.000 liệu trình Paxlovid vào cuối tháng tới và ít nhất 50 triệu liệu trình đến cuối năm 2022./.