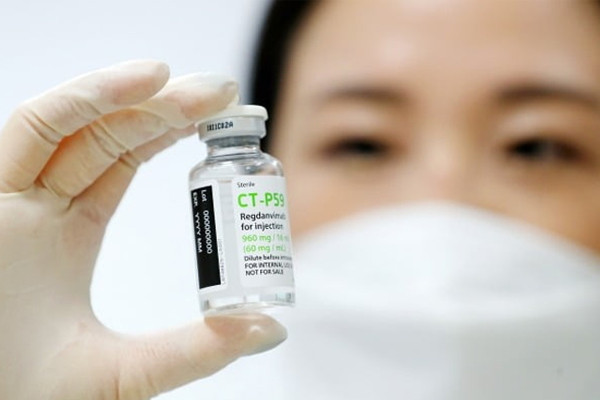
 Thuốc CT-P59. (Nguồn: Yonhap)
Thuốc CT-P59. (Nguồn: Yonhap)
Ngày 5/2, Cơ quan An toàn dược phẩm và thực phẩm Hàn Quốc cho biết đã cấp phép có điều kiện thuốc điều trị bệnh viêm đường hô hấp cấp COVID-19 bằng kháng thể đơn dòng do tập đoàn dược phẩm Celltrion sản xuất.
Như vậy, đây là thuốc điều trị đầu tiên do một công ty dược phẩm trong nước sản xuất được cấp phép tại Hàn Quốc.
Trong tuyên bố của mình, cơ quan trên cho biết đã cấp phép lưu hành đối với thuốc CT-P59 (Regkirona Inj.) với điều kiện đơn vị sản xuất là tập đoàn dược phẩm Celltrion phải nộp kết quả thử nghiệm lâm sàng giai đoạn ba trên toàn cầu.
[Hàn Quốc: Thuốc trị COVID-19 của Celltrion hiệu quả hơn của Mỹ]
Hồi tháng 12 năm ngoái, Celltrion đã nộp đơn xin cấp phép lưu hành có điều kiện đối với thuốc điều trị COVID-19 bằng kháng thể đơn dòng này.
Tháng 1 vừa qua, công ty công bố kết quả nghiên cứu lâm sàng giai đoạn hai được tiến hành trên toàn cầu, cho thấy loại thuốc này giúp giảm đáng kể nguy cơ nhập viện và phải thở máy.
CT-P59 là loại thuốc điều trị COVID-19 bằng kháng thể được sản xuất bằng cách chọn gene kháng thể trung hòa trong máu của bệnh nhân mắc COVID-19 trong thời kỳ dưỡng bệnh và đưa gene đã chọn vào tế bào chủ được nuôi cấy để sản xuất kháng thể trên quy mô lớn.
Thuốc này có thể tiêm cho bệnh nhân ngoại trú mắc COVID-19 có nguy cơ cao (gồm những người ngoài 60 tuổi hoặc có bệnh lý nền như tim mạch, tiểu đường, huyết áp cao và bệnh hô hấp mãn tính), cũng như bệnh nhân ngoại trú với các triệu chứng trung bình từ 18 tuổi trở lên.
Thuốc này có thể được tiêm trực tiếp qua tĩnh mạch trong khoảng 90 phút.
Celltrion cho biết có kế hoạch tiến hành thử nghiệm lâm sàng giai đoạn ba đối với CT-P59 tại hơn 10 nước nhằm thu được kết quả toàn diện hơn về tính an toàn và hiệu quả của CT-P59.
Công ty cũng có kế hoạch nộp đơn xin Cấp phép sử dụng khẩn cấp lên Cơ quan Quản lý thực phẩm và dược phẩm Mỹ và đơn xin Cấp phép tiếp thị có điều kiện lên Cơ quan Dược phẩm châu Âu (EMA) trong những tháng tới./.